WikiDer > Dihidroksimalon kislotasi
 | |
| Ismlar | |
|---|---|
| IUPAC nomi 2,2-Dihidroksipropandioik kislota | |
| Boshqa ismlar Dihidroksipropandioik kislota Mezoksalik kislota monohidrat Oksomalonik kislota monohidrat Ketomalonik kislota monohidrat | |
| Identifikatorlar | |
3D model (JSmol) | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.008.372 |
PubChem CID | |
| UNII | |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
| C3H4O6 | |
| Molyar massa | 136.059 g · mol−1 |
| Erish nuqtasi | 119 dan 120 ° C gacha (246 dan 248 ° F; 392 dan 393 K gacha) |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar berilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
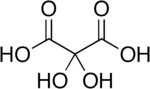
Dihidroksimalon kislotasi bu organik birikma formulasi C bilan3H4O6 yoki HO- (C = O) -C (OH)2- (C = O) -OH, kabi ba'zi o'simliklarda uchraydi beda va lavlagi pekmez.[2]
Murakkab shuningdek deyiladi dihidroksimoksoksal kislotasi va dihidroksipropandioik kislota. Buni a hidrat hosilasi mezoksalik kislota, va tez-tez chaqiriladi mezoksalik kislota monohidrat va shunga o'xshash ismlar.[3] Ushbu birikma tarkibida stabil bo'lmaganligi odatiy emas geminal gidroksi guruhlar.
Dihidroksimalon kislotasi suvda eriydigan oq qattiq moddadir. Bu kristallanadi yilda sust prizmalar suv yo'qotmasdan 113 ° C dan 121 ° C gacha eriydi.[4] Tibbiy tadqiqotlarda u sifatida ishlatilgan hipoglisemik vosita[5] va 1997 yilda tezkor harakat sifatida AQShda patentlangan antidot ga siyanid zaharlanish.[6]
Sintez
Dihidroksimalon kislotasini sintetik usul bilan olish mumkin gidroliz ning alloksan bilan barita suv,[2] isitish orqali kofe kislotasi[7] bilan qo'rg'oshin asetat yechim,[4] elektroliz bilan tartarik kislota ishqoriy eritmada,[8] yoki dan glitserin diatsetat va jamlangan azot kislotasi sovuqda. Mahsulotni oksidlanish orqali ham olish mumkin tartronik kislota[9] yoki glitserol.[10]
Reaksiyalar
Odatda gidratlangan keton kislotalari singari, u kamayadi suvli eritma tomonidan natriy amalgam ga tartronik kislota, shuningdek, bilan birlashadi fenilgidrazin va gidroksilamin. Bu kamayadi ammiakal kumush echimlar. Bilan qizdirilganda karbamid 100 ° C gacha, u hosil bo'ladi allantoin. Suvli eritmasining davomiy qaynab turishi natijasida u parchalanadi karbonat angidrid va glyoksilik kislota.
Shuningdek qarang
Adabiyotlar
- ^ Merck indeksi, 12-nashr, 5971.
- ^ a b Deyxsel, Teodor (1864). "Ueber Mesoxalsäure vafot etadi". J. Prakt. Kimyoviy. (nemis tilida). 93 (1): 193–208. doi:10.1002 / prac.18640930139.
- ^ E. T. Urbanskiy, V. J. Bashe (2000). Kromatografiya jurnali A, 867-jild, 143–149-betlar.
- ^ a b Genri Enfild Rosko (1888), Kimyo bo'yicha risola, 3-jild, 2-qism Organik kimyo, p. 161. D. Appleton and Co., Nyu-York.
- ^ Yoshito KOBAYASHI, Shigeru OHASHI, Shinzaburo TANAKA va Akitoshi SHIOYA (1955), Natriy mesoksalatning gipoglikemik ta'siriga, sovuqqa ta'sir qiladigan itlarda gipofiz-buyrak usti kortikal tizimining giperfunktsiyasiga alohida murojaat qiling.[doimiy o'lik havola]. Yaponiya akademiyasi materiallari, 31-jild, 8-son, 493-497 betlar.
- ^ Siyanid bilan zaharlanishni davolash usuli
- ^ Kofur kislotasining kimyoviy tuzilishi Allen, W. F. (1932) da berilgan. 8-efir kofeinning tayyorlanishi va pirolitik molekulyar qayta tashkil etilishi: Va ularning 8-metil va 8-etilkofeinga aylanishi. Ann Arbor, Mich.: Birodarlar Edvards.
- ^ (1922), kimyoviy. Zentralblatt III, 871
- ^ Ciriminna, Rosaria (2004). "TEMPO vositachiligida tartronik kislota va dihidroksietonni natriy mezoksalatga oksidlash". Tetraedr xatlari. 45 (34): 6381–6383. doi:10.1016 / j.tetlet.2004.07.021.
- ^ Ciriminna, Rosaria (2003). "TEMPO vositachiligida glitserolni ketomalon kislotasiga bir qozonli va bir hil bo'lmagan oksidlanish". Kengaytirilgan sintez va kataliz. 345 (3): 383–388. doi:10.1002 / adsc.200390043.