WikiDer > Vanadiy tetraflorid
| Ismlar | |||
|---|---|---|---|
| IUPAC nomi vanadiy tetraflorid | |||
| Identifikatorlar | |||
3D model (JSmol) | |||
| ChemSpider | |||
| ECHA ma'lumot kartasi | 100.030.143 | ||
| EC raqami |
| ||
PubChem CID | |||
| UNII | |||
| BMT raqami | UN2923 | ||
CompTox boshqaruv paneli (EPA) | |||
| |||
| |||
| Xususiyatlari | |||
| F4V | |||
| Molyar massa | 126.9351 g · mol−1 | ||
| Tashqi ko'rinish | Ohak kukuni, gigroskopik[1] | ||
| Hidi | Hidi yo'q | ||
| Zichlik | 3.15 g / sm3 (20 ° C)[1] 2.975 g / sm3 (23 ° C)[2] | ||
| Erish nuqtasi | 325 ° C (617 ° F; 598 K) 760 mm simob ustuni parchalanadi[1] | ||
| Qaynatish nuqtasi | Sublimes[1] | ||
| Juda eriydi[1] | |||
| Eriydiganlik | Eriydi aseton, sirka kislotasi Juda oz eriydi SO2Cl2, spirtli ichimliklar, CHCl3[2] | ||
| Tuzilishi | |||
| Monoklinik, mP10 | |||
| P21/ c, № 14 | |||
| Termokimyo | |||
Std molar entropiya (S | 126 J / mol · K[3] | ||
Std entalpiyasi shakllanish (ΔfH⦵298) | -1412 kJ / mol[3] | ||
Gibbs bepul energiya (ΔfG˚) | -1312 kJ / mol[3] | ||
| Xavf | |||
| GHS piktogrammalari |   [4] [4] | ||
| GHS signal so'zi | Xavfli | ||
| H300, H330, H314, H318[4] | |||
| P260, P301 + 310, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P320, P330, P405, P501[4] | |||
| Ko'z xavf | Jiddiy zarar etkazadi | ||
| Teri xavf | Kuyish sabab bo'ladi | ||
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar berilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |||
| Infobox ma'lumotnomalari | |||
Vanadiy (IV) ftor (VF4) an noorganik birikma ning vanadiy va ftor. Bu paramagnetik sariq-jigarrang qattiq gigroskopik.[2] Tegishli narsadan farqli o'laroq vanadiy tetraklorid, tetraflorid uchuvchan emas, chunki u polimer tuzilishini qabul qiladi. U eritishdan oldin parchalanadi.
Tayyorlanishi va reaktsiyalari
VF4 VCl ni davolash orqali tayyorlash mumkin4 bilan HF:
- VCl4 + 4 HF → VF4 + 4 HCl
Dastlab shu tarzda tayyorlandi.[5]
U 325 ° C da parchalanib, ga nisbatan nomutanosiblikka uchraydi uch va pentafloridlar:[2]
- 2 VF4 → VF3 + VF5
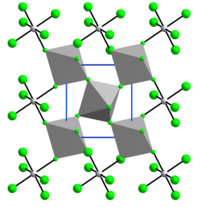
Tuzilishi
VFning tuzilishi4 bilan bog'liq SnF4. Har bir vanadiy markazi oltita florid ligand bilan o'ralgan, oktahedraldir. Ftorli markazlarning to'rttasi ko'prik qo'shni vanadiy markazlariga.[6]
Adabiyotlar
- ^ a b v d e Lide, Devid R., ed. (2009). CRC Kimyo va fizika bo'yicha qo'llanma (90-nashr). Boka-Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ^ a b v d Kvasnik, V. (1963). Brauer, Georg (tahrir). Preparat noorganik kimyo bo'yicha qo'llanma (Buyuk Britaniya tahr.). London: Academic Press. pp.252–253.
- ^ a b v Anatolievich, Kiper Ruslan. "vanadiy (IV) ftor". http://chemister.ru. Olingan 2014-06-25. Tashqi havola
| veb-sayt =(Yordam bering) - ^ a b v "Vanadiy (IV) ftor, 95%". http://www.alfa.com. Alfa Aesar. Olingan 2014-06-25. Tashqi havola
| veb-sayt =(Yordam bering) - ^ Otto Ruff, Gerbert Likfett "Vanadinfluoride" Chemische Berichte 1911, jild. 44, 2539–2549 betlar. doi:10.1002 / cber.19110440379
- ^ Beker S., Myuller B. G. Tetrafloridli vanadiy, Angev. Kimyoviy. Intnl. Ed. Ingl. 1990 yil, jild 29, 406-bet
- Veb-elementlar
- Paxta, F. Albert; Uilkinson, Jefri; Murillo, Karlos A .; Bochmann, Manfred (1999), Ilg'or anorganik kimyo (6-nashr), Nyu-York: Wiley-Interscience, ISBN 0-471-19957-5
| Bu noorganik birikma- tegishli maqola a naycha. Siz Vikipediyaga yordam berishingiz mumkin uni kengaytirish. |