WikiDer > Romidepsin
 | |
 | |
| Klinik ma'lumotlar | |
|---|---|
| Savdo nomlari | Istodax |
| Boshqa ismlar | FK228; FR901228; Istodax |
| MedlinePlus | a610005 |
| Litsenziya ma'lumotlari |
|
| Homiladorlik toifasi |
|
| Marshrutlari ma'muriyat | Vena ichiga yuborish |
| ATC kodi | |
| Huquqiy holat | |
| Huquqiy holat |
|
| Farmakokinetik ma'lumotlar | |
| Bioavailability | Qo'llash mumkin emas (faqat IV) |
| Protein bilan bog'lanish | 92–94% |
| Metabolizm | Jigar (asosan CYP3A4vositachilik) |
| Yo'q qilish yarim hayot | 3 soat |
| Identifikatorlar | |
| |
| CAS raqami | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| ChEBI | |
| ChEMBL | |
| CompTox boshqaruv paneli (EPA) | |
| ECHA ma'lumot kartasi | 100.211.884 |
| Kimyoviy va fizik ma'lumotlar | |
| Formula | C24H36N4O6S2 |
| Molyar massa | 540.69 g · mol−1 |
| 3D model (JSmol) | |
| |
| |
| | |
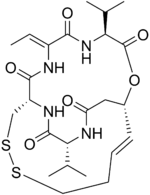
Romidepsin, shuningdek, nomi bilan tanilgan Istodax, bu saratonga qarshi vosita ichida ishlatilgan teri T-hujayrali limfoma (CTCL) va boshqalar periferik T-hujayrali limfomalar (PTCL). Romidepsin a tabiiy mahsulot bakteriyadan olingan Chromobacterium vioaceumva ma'lum bo'lgan fermentlarni blokirovka qilish orqali ishlaydi giston deatsetilazalari, shunday qilib induktsiya qilish apoptoz.[1] Ba'zan u deb nomlanadi depsipeptid, u tegishli bo'lgan molekulalar sinfidan keyin. Romidepsin markasi va Gloucester Pharmaceuticals kompaniyasiga tegishli, endi uning bir qismi Selgen.[2]
Tarix
Romidepsin haqida birinchi marta 1994 yilda Fujisawa Farmatsevtika Kompaniyasining tadqiqotchilari guruhi tomonidan ilmiy adabiyotlarda xabar berilgan. Astellas Pharma) ichida Tsukuba, Yaponiya, kim uni madaniyatida ajratgan Chromobacterium vioaceum olingan tuproq namunasidan Yamagata prefekturasi.[3] Antibakterial ta'sirga ega bo'lmaganligi aniqlandi, ammo u kuchli edi sitotoksik bir nechta odamga qarshi saraton hujayra chiziqlari, oddiy hujayralarga ta'siri yo'q; sichqonlar ustida olib borilgan tadqiqotlar keyinchalik antitümör faolligini topdi jonli ravishda shuningdek.[3]
Birinchi umumiy sintez romidepsin tomonidan bajarilgan Garvard tadqiqotchilar va 1996 yilda nashr etilgan.[4] Uning ta'sir mexanizmi 1998 yilda, Fujisava va Tokio universiteti a ekanligini aniqladi giston deatsetilaza inhibitori ta'siriga o'xshash effektlar bilan trichostatin A.[5]
Klinik sinovlar
I bosqich dastlab FK228 va FR901228 kodlari bilan nomlangan romidepsinni o'rganish 1997 yilda boshlangan.[6] II bosqich va III bosqich sinovlari turli ko'rsatkichlar bo'yicha o'tkazildi. Davolashda eng muhim natijalar aniqlandi teri T-hujayrali limfoma (CTCL) va boshqalar periferik T-hujayrali limfomalar (PTCL).[6]
2004 yilda romidepsin qabul qildi Tezkor trek teri hujayralari T-hujayrasi lenfomasini davolash uchun FDA tomonidan belgilanishi va yetim dori FDA va holati Evropa dorilar agentligi xuddi shu ko'rsatkich uchun.[6]
FDA 2009 yil noyabr oyida CTCL uchun romidepsinni ma'qulladi[7] va boshqalar uchun tasdiqlangan romidepsin periferik T-hujayrali limfomalar (PTCL) 2011 yil iyun oyida.[8]
Klinikadan oldin OIVni o'rganish
2014 yilda, PLOS patogenlari OIV rezervuarini tugatish uchun yashirin OIV virusini qayta faollashtirishga mo'ljallangan sinovda romidepsin ishtirokidagi tadqiqotni nashr etdi. Yashirin yuqtirilgan T hujayralari fosh qilindi in vitro va ex vivo romidepsinga, bu hujayralar bilan bog'liq bo'lgan OIV RNKning aniqlanadigan darajasining oshishiga olib keladi. Sinov shuningdek, romidepsin ta'sirini boshqa histon deatsetilaza inhibitori bilan taqqosladi, Vorinostat [9]
Autizmni hayvon modelida o'rganish
Romidepsinni hayvonlarni o'rganishda ishtirok etgan tadqiqot shuni ko'rsatdiki, kam miqdordagi romidepsin bilan qisqa muddatli davolanish autizmning sichqoncha modelidagi ijtimoiy nuqsonlarni qaytarishi mumkin.[10]
Farmakodinamika
CTCL yoki PTCL bilan og'rigan bemorlarni o'z ichiga olgan romidepsinning II bosqichida o'tkazilgan sinovda, periferik qon mononukleer hujayralarida (PBMC) 4-48 soat davom etgan giston atsetilatsiyasining ko'payganligi to'g'risida dalillar mavjud. Romidepsin bilan indikatsiyalangan gen ekspressionining markeri bo'lgan ABCB1 genining ekspressioni ham PBMClarda, ham o'smaning biopsiya namunalarida ko'paygan. Giston atsetilatsiyasining ortishi ortib borayotgan gen ekspressioni HDAC inhibitori kutilgan ta'siridir. Qonda romidepsin kiritilgandan so'ng gemoglobin F ning ko'payishi (HDAC inhibatsiyasi natijasida kelib chiqadigan gen ekspression o'zgarishi uchun yana bir surrogat marker) aniqlandi va doimiy histon asetilatsiyasi dori-darmonlarni tozalash bilan teskari bog'liq bo'lib, bemorning terapiyaga javobi bilan bevosita bog'liq.[11]
Dozalash va qabul qilish
Ham CTCL, ham PTCLda romidepsinning tasdiqlangan dozasi to'rt soatlik i.v. 28 kunlik davolash tsiklining 1, 8 va 15 kunlarida 14 mg / m2 miqdorida yuborish.[12] Ushbu tsikl, agar bemor terapiyadan foyda ko'rsa va toqat qilsa, uni takrorlash kerak. Yuqori toksik ta'sirga ega bo'lgan ayrim bemorlarda dozani 10 mg / m2 gacha kamaytirish mumkin.
Farmakokinetikasi
Rivitepsin saraton kasalligi yuqori bo'lgan bemorlarni o'z ichiga olgan sinovlarda to'rt soat davomida tomir ichiga yuborilganda 1,0 dan 24,9 mg / m2 gacha bo'lgan dozalarda chiziqli farmakokinetikani namoyish etdi.[13] Yoshi, irqi, jinsi, buyrak etishmovchiligining og'irligi va jigarning engil-o'rta darajadagi buzilishi romidepsin farmakokinetikasiga ta'sir ko'rsatmadi. Qayta dozalashdan keyin plazmadagi konsentratsiyaning to'planishi kuzatilmadi.[14]
Ta'sir mexanizmi
Romidepsin a vazifasini bajaradi oldingi dori bilan disulfid birikmasi o'tmoqda kamaytirish hujayra ichida rux bilan bog'laydigan moddalarni chiqarish uchun tiol.[3][15][16] Tiol Znga bog'liq bo'lgan majburiy cho'ntagida sink atomiga bog'lanadi giston deatsetilaza uning faoliyatini blokirovka qilish. Shunday qilib u HDAC inhibitori. Ko'pchilik HDAC inhibitörleri epigenetik ravishda o'smaning supressor genlarining normal ekspressionini tiklash qobiliyati orqali saraton kasalligini davolash mumkin, bu hujayralar tsiklini to'xtatish, differentsiatsiya va apoptoz.[17]
Yomon ta'sir
Romidepsinni ishlatish bir xil bilan bog'liq salbiy ta'sir.[18] Klinik tadkikotlarda eng keng tarqalgani ko'ngil aynish va qusish, charchoq, infektsiya, ishtahani yo'qotishva qon kasalliklari (shu jumladan anemiya, trombotsitopeniyava leykopeniya). Bu shuningdek infektsiyalar va metabolizmning buzilishi (masalan, g'ayritabiiy) bilan bog'liq elektrolit darajalari), teri reaktsiyalari, ta'mni idrok etishning o'zgarishiva o'zgarishlar yurak elektr o'tkazuvchanligi.[18]
Adabiyotlar
- ^ "Romidepsin". Milliy saraton instituti. Olingan 2009-09-11.
- ^ "Romidepsin". Gloucester farmatsevtikasi. Olingan 2009-09-11.[doimiy o'lik havola]
- ^ a b v Ueda H, Nakajima H, Xori Y va boshqalar. (1994 yil mart). "FR901228, yangi antitumor bitsiklik depsipeptid tomonidan ishlab chiqarilgan Chromobacterium vioaceum № 968. I. Taksonomiya, fermentatsiya, izolyatsiya, fizik-kimyoviy va biologik xususiyatlar va o'smaga qarshi faollik ". Antibiotiklar jurnali. 47 (3): 301–10. doi:10.7164 / antibiotiklar. 47.301. PMID 7513682.
- ^ Li KV, Vu J, Xing V, Simon JA (1996 yil iyul). "FR-901,228 antitumor depsipeptidning umumiy sintezi". Amerika Kimyo Jamiyati jurnali. 118 (30): 7237–8. doi:10.1021 / ja9613724.
- ^ Nakajima H, Kim YB, Terano H, Yoshida M, Horinouchi S (may 1998). "FR901228, kuchli antitumor antibiotik, yangi histon deatsetilaza inhibitori". Eksperimental hujayra tadqiqotlari. 241 (1): 126–33. doi:10.1006 / excr.1998.4027. PMID 9633520.
- ^ a b v Masuoka Y, Shindoh N, Inamura N (2008). "Mikroorganizmlardan histon deatsetilaza inhibitörleri: Astellas tajribasi". Petersen F, Amstutz R (tahr.). Tabiiy birikmalar dori sifatida. 2. Bazel: Birkxauzer. 335-59 betlar. ISBN 978-3-7643-8594-1. 2009 yil 8-noyabrda olingan Google Book Search.
- ^ http://chembl.blogspot.com/2009/11/new-drug-approvals-pt-xxiii-romidepsin.html
- ^ http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index.cfm?fuseaction=Reports.MonthlyApprovalsAll
- ^ Vey, D; va boshq. (2014). "Giston deatsetilaza inhibitori Romidepsin Klinik dozalash natijasida erishilgan konsentrasiyalarda antressetrovirus virusli terapiya bo'yicha bemorlarning CD4 T hujayralarida OIV ekspresiyasini keltirib chiqaradi". PLoS Pathog. 10 (4): e1004071. doi:10.1371 / journal.ppat.1004071. PMC 3983056. PMID 24722454.
- ^ Tsin, Lyuy; Ma, Kaijie; Vang, Zi-Jun; Xu, Sixua; Matas, Emmanuel; Vey, Jing; Yan, Zhen (2018). "Shank3 etishmovchiligi bo'lgan autizmning sichqon modellarida ijtimoiy nuqsonlar histon deatsetilaza (HDAC) inhibisyoni yordamida qutqariladi". Tabiat nevrologiyasi. 21 (4): 564. doi:10.1038 / s41593-018-0110-8. PMC 5876144. PMID 29531362.
- ^ Beyts, Syuzan E .; Zhan, Zhirong; Steydman, Kennet; Obrzut, Tomash; Luchenko, Viktoriya; Fray, Robin; Robi, Robert V.; Tyorner, Mariya; Gardner, Erin R. (2010 yil yanvar). "Laboratoriya Teri va periferik T-hujayrali limfomada romidepsinni II bosqich sinovi bilan bog'liq". Britaniya gematologiya jurnali. 148 (2): 256–267. doi:10.1111 / j.1365-2141.2009.07954.x. ISSN 0007-1048. PMC 2838427. PMID 19874311.
- ^ Nakajima, Xidenori; Kim, Young Bae; Terano, Xirosi; Yoshida, Minoru; Horinouchi, Sueharu (may, 1998). "FR901228, kuchli antitumor antibiotik, bu roman histon deatsetilaza inhibitori". Eksperimental hujayra tadqiqotlari. 241 (1): 126–133. doi:10.1006 / excr.1998.4027. ISSN 0014-4827. PMID 9633520.
- ^ Bredner, Jeyms E; G'arbiy, Natan; Grachan, Melissa L; Grinberg, Edvard F; Xaggarti, Stiven J; Warnow, Tandy; Mazitschek, Ralf (2010-02-07). "Giston deatsetilazalarning kimyoviy filogenetikasi". Tabiat kimyoviy biologiyasi. 6 (3): 238–243. doi:10.1038 / nchembio.313. ISSN 1552-4450. PMC 2822059. PMID 20139990.
- ^ Nakajima, Xidenori; Kim, Young Bae; Terano, Xirosi; Yoshida, Minoru; Horinouchi, Sueharu (may, 1998). "FR901228, kuchli antitumor antibiotik, bu roman histon deatsetilaza inhibitori". Eksperimental hujayra tadqiqotlari. 241 (1): 126–133. doi:10.1006 / excr.1998.4027. ISSN 0014-4827. PMID 9633520.
- ^ Shigematsu, N .; Ueda, X.; Takase, S .; Tanaka, X.; Yamamoto, K .; Tada, T. (1994). "FR901228, 968-sonli Chromobacterium vioaceum tomonidan ishlab chiqarilgan antitumor bitsiklik depsipeptid. II. Tuzilishini aniqlash". J. Antibiot. 47 (3): 311–314. doi:10.7164 / antibiotiklar.47.311. PMID 8175483.
- ^ Ueda, X.; Manda, T .; Matsumoto, S .; Mukumoto, S .; Nishigaki, F.; Kavamura, men.; Shimomura, K. (1994). "FR901228, 968-sonli Chromobacterium vioaceum tomonidan ishlab chiqarilgan yangi antitumor bisiklik depsipeptid. III. Sichqonlardagi eksperimental o'smalarga qarshi antitumor harakatlar". J. Antibiot. 47 (3): 315–323. doi:10.7164 / antibiotiklar.47.315. PMID 8175484.
- ^ Gresok, Tomas J.; Jons, Deyrid M.; Noguchi, Yasuo; Uilyams, Robert M. (2008). "Potentsial HDAC inhibitori FK228 (FR-901228) ning umumiy sintezi". Organik xatlar. 10 (4): 613–616. doi:10.1021 / ol702957z. PMC 3097137. PMID 18205373.
- ^ a b [Mualliflar ro'yxati yo'q] (2014 yil oktyabr). "ISTODEX yorlig'i haqida ma'lumot (2014 yil oktyabrgacha yangilangan)" (PDF). AQSh oziq-ovqat va farmatsevtika idorasi.